17/05/2025
El Universo Mecánico: Analizando la Ley de los Gases
Las leyes de los gases son pilares fundamentales en la comprensión del comportamiento de la materia en estado gaseoso. Estas leyes, incluyendo la ley de Boyle-Mariotte, la ley de Gay-Lussac, la ley de Charles y la ley de Avogadro, nos permiten predecir y explicar cómo los gases responden a cambios en variables como la temperatura, la presión y el volumen.
Profundizando en las Leyes Fundamentales de los Gases
Ley de Avogadro: Esta ley establece una relación directa entre la cantidad de sustancia (moles) de un gas y su volumen, manteniendo la temperatura y presión constantes. Volúmenes iguales de diferentes gases, bajo las mismas condiciones de temperatura y presión, contienen el mismo número de partículas. La ecuación V/n = k, donde V es volumen, n es la cantidad de sustancia y k es una constante, resume este principio.
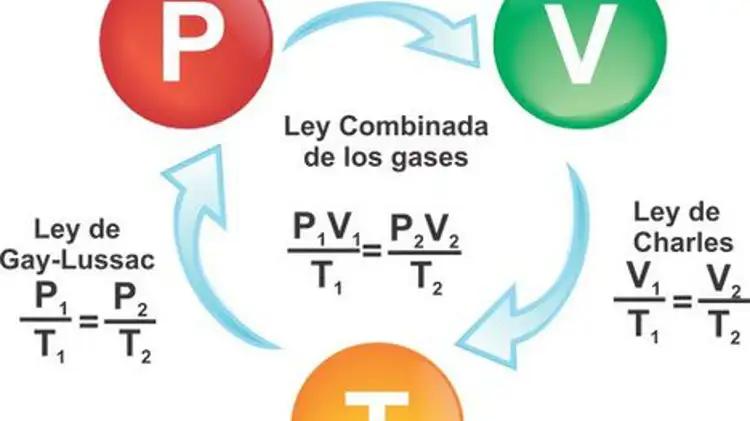
Ley de Boyle-Mariotte: A temperatura constante, el producto de la presión y el volumen de una cantidad fija de gas permanece constante. En otras palabras, si la presión aumenta, el volumen disminuye, y viceversa. La ecuación P₁ ∙ V₁ = P₂ ∙ V₂ ilustra esta relación, donde P₁ y V₁ representan la presión y volumen iniciales, y P₂ y V₂ la presión y volumen finales.
Ley de Charles: Esta ley describe la relación directa entre el volumen y la temperatura de un gas a presión constante. A medida que la temperatura aumenta, el volumen también aumenta, y viceversa. La ecuación V₁ / T₁ = V₂ / T₂ representa esta ley, donde V₁ y T₁ son el volumen y la temperatura iniciales, y V₂ y T₂ el volumen y la temperatura finales.
Ley de Gay-Lussac: A volumen constante, la presión de un gas es directamente proporcional a su temperatura en Kelvin. Si la temperatura aumenta, la presión también aumenta, y viceversa. La ecuación P₁ / T₁ = P₂ / T₂ describe esta relación, donde P₁ y T₁ son la presión y temperatura iniciales, y P₂ y T₂ la presión y temperatura finales.
El Origen de las Leyes de los Gases: Un Viaje a Través de la Historia
El descubrimiento de estas leyes se remonta a siglos atrás, con figuras clave como Robert Boyle, Edme Mariotte, Jacques Charles, Joseph Louis Gay-Lussac y Amedeo Avogadro. Cada uno de estos científicos contribuyó con observaciones y experimentos que llevaron a la formulación de las leyes que rigen el comportamiento de los gases.
La Ecuación de Estado de los Gases Ideales: Un Modelo Fundamental
La ecuación de estado de los gases ideales, PV = nRT, combina las leyes de los gases ideales en una sola expresión. Esta ecuación relaciona la presión (P), el volumen (V), la cantidad de sustancia (n), la constante de los gases ideales (R) y la temperatura (T) de un gas ideal. Es importante destacar que esta ecuación se aplica a gases ideales, que son modelos teóricos que no consideran las interacciones intermoleculares ni el volumen de las partículas.
Consideraciones para Gases Reales: Desviaciones del Comportamiento Ideal
En condiciones de alta presión o baja temperatura, los gases reales pueden desviarse significativamente del comportamiento predicho por la ecuación de los gases ideales. Esto se debe a que las interacciones intermoleculares y el volumen de las partículas del gas se vuelven más relevantes en estas condiciones. Para describir con precisión el comportamiento de los gases reales, se requieren ecuaciones de estado más complejas.
Isotermas: Visualizando la Relación Presión-Volumen
Las isotermas son curvas que representan la relación entre la presión y el volumen de un gas a temperatura constante. Estas curvas son útiles para visualizar cómo cambia el comportamiento de un gas bajo diferentes condiciones de presión, manteniendo la temperatura constante.
 Aplicaciones Prácticas de las Leyes de los Gases
Aplicaciones Prácticas de las Leyes de los Gases
Las leyes de los gases tienen una amplia gama de aplicaciones en diversos campos, incluyendo la industria química, la investigación científica, la navegación aérea y espacial, y la meteorología. Estas leyes son herramientas esenciales para comprender y predecir el comportamiento de los gases en diferentes situaciones.
Consultas Habituales sobre la Ley de los Gases
¿Qué es un gas ideal? Un gas ideal es un modelo teórico que se utiliza para simplificar el estudio del comportamiento de los gases. Se asume que las partículas de un gas ideal no tienen volumen y no interactúan entre sí.

¿Cuándo se desvían los gases reales del comportamiento ideal? Los gases reales se desvían del comportamiento ideal a altas presiones o bajas temperaturas, cuando las interacciones intermoleculares y el volumen de las partículas se vuelven significativos.

¿Cómo se relaciona la ley de los gases con la termodinámica? La ley de los gases es una parte fundamental de la termodinámica, que estudia las relaciones entre el calor, el trabajo y la energía en los sistemas físicos.
Tabla Comparativa de las Leyes de los Gases
| Ley | Descripción | Ecuación |
|---|---|---|
| Ley de Avogadro | Relación entre cantidad de sustancia y volumen | V/n = k |
| Ley de Boyle-Mariotte | Relación entre presión y volumen | P₁ ∙ V₁ = P₂ ∙ V₂ |
| Ley de Charles | Relación entre volumen y temperatura | V₁ / T₁ = V₂ / T₂ |
| Ley de Gay-Lussac | Relación entre presión y temperatura | P₁ / T₁ = P₂ / T₂ |
Lista de Conceptos Clave
- Presión
- Volumen
- Temperatura
- Cantidad de sustancia (moles)
- Constante de los gases ideales
- Gas ideal
- Gas real
- Isoterma
Las leyes de los gases son herramientas fundamentales para comprender el comportamiento de la materia en estado gaseoso. Estas leyes, junto con la ecuación de estado de los gases ideales, proporcionan un marco teórico para predecir y explicar cómo los gases responden a cambios en las condiciones ambientales. El estudio de las leyes de los gases es esencial en una variedad de campos, desde la ciencia básica hasta la ingeniería y la tecnología.
Si quieres conocer otros artículos parecidos a El universo mecánico: ley de los gases puedes visitar la categoría Física.

